Оценка эффективности лечения хондроитин сульфатом (Артрадолом) спортсменов с посттравматической хондропатией коленных суставов
Введение
Лечение посттравматических дегенеративно-дистрофических заболеваний коленных суставов у спортсменов является актуальной проблемой спортивной медицины. Посттравматический гонартроз - одно из наиболее частых и тяжелых осложнений травм коленных суставов. Осложнения в виде посттравматического гонартроза встречаются в 35,5-69,75% случаев и развиваются в среднем через 3-5 лет после травмы [3, 24]. Основа развития посттравматического гонартроза - повреждение суставного гиалинового хряща [7, 12, 19, 20]. Одним из факторов, способствующих началу развития патологического процесса в нем, является чрезмерная, значительно превосходящая физиологическую, механическая нагрузка на суставной хрящ [21]. В результате воздействия травмирующего фактора происходит истончение, разволокнение суставного хряща, развивается посттравматическая хондропатия.
Другим фактором риска развития гонартроза является слабость периартикулярных мышц [7]. В последние годы растет число работ, подтверждающих, что снижение силы и нарушение проприорецепции четырехглавой мышцы бедра, выполняющей главную стабилизирующую функцию коленного сустава, способствуют развитию остеоартроза коленных суставов [13, 16, 18]. Исследования показали, что среди женщин без рентгенологических признаков гонартроза в начале наблюдения и с рентгенологически диагностированным остеоартрозом через 30 мес. исходная сила разгибателя колена была значительно меньше (р<0,04), чем у тех женщин, у которых не развился остеоартроз.
Было определено, что повышение силы разгибателя колена на каждые 10 фунтов/фут2 ассоциировано со снижением вероятности развития остеоартроза коленного сустава на 20%, манифестного остеоартроза - на 29% [23]. Относительно небольшое увеличение силы разгибателя колена (приблизительно на 20% от среднего для мужчин и на 25% от среднего для женщин) ассоциировано со снижением риска развития гонартроза на 20 и 30% соответственно. Таким образом, состояние параартикулярных мышц имеет огромное значение для функционирования коленного сустава [1].
Восстановительное лечение спортсменов с посттравматической хондропатией должно быть комплексным и включать медикаментозные средства и немедикаментозные методы (лечебная физкультура, массаж, физиотерапевтическое лечение). Необходимые условия успешной терапии повреждений суставного хряща, а также профилактики развития посттравматического гонартроза - как можно более раннее начало и адекватное лечение [7, 15].
Одним из направлений медикаментозной терапии дегенеративных заболеваний коленного сустава является применение хондропротекторов. Хондропротекторы - это группа препаратов, обладающих симптом-модифицирующим и, предположительно, структурно-модифицирующим действием. Типичным представителем этой группы препаратов является хондроитина сульфат. Он входит в состав суставного хряща, выполняя важнейшие обменные и биомеханические функции. Являясь естественным компонентом элементов хряща, играет биологически активную роль во многих процессах метаболизма различных структур сустава [14]. По химическому строению молекула ХС является сульфатированным глюкозаминогликаном, состоящим из длинных неразветвленных цепей с повторяющимися остатками N-ацетилгалактозамина и глюкуроновой кислоты. Подобное строение молекулы хондроитин сульфата обусловливает ее полианионные свойства и участие в процессах транспорта воды, аминокислот и липидов в аваскулярных участках хряща.
На начальном этапе исследования у хондроитин сульфата были выявлены анаболические свойства, он долгое время рассматривался как своего рода строительный материал, способствующий регенерации очага повреждения суставного хряща. Однако в последующих исследованиях было выявлено, что механизм действия хондроитин сульфата не только обусловлен способностью к повышению синтеза коллагена 2, протеогликанов и гиалуроновой кислоты, но и оказывает влияние на самые разные звенья патогенеза остеоартроза.
В ряде исследований был выявлен противовоспалительный эффект: отмечалось снижение инфильтрации воспалительными клетками синовиальной мембраны и степени ее пролиферации. Также хондроитин сульфат способен подавлять активность матриксных металлопротеиназ, принимающих участие в воспалительных реакциях, деградации костной и хрящевой ткани; обладает и антиоксидантными свойствами, подавляя реакцию окисления протеинов, перекисного окисления липидов и образование свободных радикалов. До настоящего времени изучены не все механизмы действия хондропротекторов, но положительное влияние этих препаратов на хрящевую ткань демонстрируют многочисленные клинические испытания [22, 25].
Необходимо отметить, что эффективность хондроитин сульфата возрастает при использовании довольно длительных курсов лечения (4-6 нед., не менее 2 р./год), а в большей мере положительный результат наблюдается при применении на ранних стадиях развития дегенеративно-дистрофических процессов в суставе. Особого внимания заслуживает инъекционная форма хондроитин сульфата - Артрадол. Артрадол представляет собой лиофилизированный порошок для внутримышечных инъекций, его преимуществами являются большая биодоступность и хорошая переносимость.
Цель исследования: оценить в сравнительном аспекте эффективность лечения хондроитин сульфатом (Артрадолом) спортсменов с посттравматической хондропатией коленных суставов.
Материалы и методы исследования
В исследовании приняли участие 60 спортсменов, занимающихся игровыми видами спорта (футбол, гандбол, волейбол) и имеющих различную спортивную квалификацию (от 1 взр. до МСМК), с посттравматической хондропатией коленных суставов. Средний возраст спортсменов составил 25,8±7,2 года, стаж занятий спортом - 12±4 года.
Всех спортсменов мы разделили на 2 группы, сопоставимые по полу, возрасту и степени структурных изменений в травмированных коленных суставах. Основная группа (n=30) прошла курс лечения препаратом Артрадол (внутримышечно 30 инъекций через день, по схеме согласно инструкции), группа сравнения (n=30) - курс физиотерапевтического лечения переменным магнитным полем на область травмированного коленного сустава.
Для изучения субъективной оценки функционального состояния поврежденного коленного сустава использовали шкалу оценки исходов повреждений и заболеваний коленного сустава - КООS (Кnее injury and osteoarthritis outcome score), разработанную Е. Rооs (Departament of Ortopedics, Lund University Hospital, Sweden) для оценки функции коленного сустава в повседневной и активной спортивной жизни [7, 8]. Шкала КООS сочетает в себе черты шкал WОМАС, SF-36 и позволяет оценить степень болевого синдрома, нарушения функции пораженного сустава и влияние заболевания на качество жизни пациента. Отличительной особенностью шкалы КООS является возможность самооценки влияния заболевания на спортивную деятельность, что позволяет применять ее в практике спортивной медицины. Шкала состоит из 5 подразделов: «Боль», «Симптомы», «Сложность выполнения ежедневных бытовых действий», «Спорт, активность на отдыхе», «Качество жизни». В соответствии с цифровым значением от 0 до 4 подсчитывали количество полученных баллов. Затем с помощью формул производили нормализацию показателей с учетом максимальных значений по каждой субшкале в отдельности и вычисление итогового индекса в целом. Оценка показателя: наилучшая ситуация (отсутствие признака) - значение стремится к 100, наихудшая (максимальная степень выраженности признака) - значение стремится к 0.
Состояние гиалинового хряща коленных суставов оценивали методом ультрасонографии, т.к. данный метод является достаточно информативным в диагностике состояния мягкотканных структур, гиалинового хряща и менисков, что подтверждено сравнительной оценкой данных УЗИ и магнитно-резонансной томографии (МРТ) [4-6, 11]. Исследование проводили на аппарате Tochiba, Samsung Sonoace R3 с использованием высокочастотного линейного датчика с частотой 7,5-10,0 МГц.
Оценивали структуру и толщину гиалинового хряща мыщелков бедренной кости травмированного коленного сустава с вычислением индекса дегенеративного истончения хряща (ИДИХ). Основными зонами для оценки толщины и структуры хряща бедренной кости являлись нагружаемая поверхность в продольной инфрапателлярной проекции в положении сгибания в коленном суставе под углом 90° и задняя поверхность мыщелков бедренной кости в продольной (медиальной и латеральной) подколенной проекции. ИДИХ вычисляли путем отношения толщины гиалинового хряща нагружаемой поверхности к толщине хряща задней поверхности мыщелка бедренной кости. Структурные изменения гиалинового хряща оценивали в соответствии с классификацией, приближенной к классификации ICRS (International Cartilage Repair Society), на основе классификации Outerbridg (1961), дополненной и модифицированной для ультразвуковой диагностики [9]. В этой классификации выделяют 4 степени дегенеративных изменений, или хондромаляции:
- 0 - нормальный хрящ;
- 1-я степень - повышение эхогенности, однородная структура, четкий, умеренно неровный контур, обычной толщины;
- 2-я степень - повышение эхогенности, неоднородная структура, нечеткий, неровный контур, истончение в нагружаемых отделах менее 50%, ИДИХ 0,5-0,8;
- 3-я степень - повышение эхогенности, неоднородная структура, нечеткий, выраженно неровный эрозиро- ванный контур, значительное истончение в нагружаемых отделах, ИДИХ менее 0,5;
- 4-я степень - добавляются обширные зоны отсутствия хряща.
Ультразвуковыми признаками посттравматической хондропатии коленного сустава являлись диффузное повышение эхогенности, неровный, нечеткий контур, истончение в нагружаемых отделах мыщелков бедренной кости.
В качестве референтного метода нами использовалась МРТ [2, 10]. МРТ-исследование выполнено на аппарате Magnetom Symphony фирмы Siemens (Германия) 1,5 Тс. по программам рd+T2 TSE, pd TSE fs, T1 TSE, T2 me2d в аксиальной, коронарной и сагиттальной плоскостях с толщиной срезов 3 мм. Результаты МРТ-исследования коленных суставов проведены 10 спортсменам и сопоставлены с данными, полученными при ультразвуковом обследовании. Сравнение данных УЗИ и МРТ показало сопоставимость методов в выявлении изменения суставного хряща.
С целью объективной оценки функционального состояния коленных суставов у спортсменов с посттравматической хондропатией применяли метод изокинетической динамометрии мышц разгибателей голени (четырехглавой мышцы бедра) с применением системы Biodex System 4 Рrо (США). Исследование выполнялось по следующему протоколу: режим работы - изокинетический, тестирование двустороннее - на угловых скоростях 60, 180, 300°, количество повторений - 5, 10 и 15 соответственно. Для универсальной оценки использовали соотношение пикового вращающего момента к весу тела (ПВМ/ВТ).
Перед началом тестирования проводили обучение спортсменов методике работы на системе Biodex System 4 Рrо , разминку, индивидуальную стабилизацию исследуемого в кресле пациента, калибровку системы. Тестирование начинали с пораженного коленного сустава. Сравнительную оценку полученных результатов динамометрии проводили с аналогичными показателями интактной конечности. Критерии оценки: дефицит 1-10% - незначительный, коррекции не требует; 11-25% - умеренные отклонения, рекомендована реабилитация для улучшения мышечного баланса; >25% - значительные функциональные нарушения, требуют активного лечения.
Статистическая обработка и оценка достоверности различий полученных результатов проводились с вычислением 1-критерия Стьюдента.
Исследование проведено с соблюдением прав, предусмотренных ст. 7 Международной конвенции гражданских и политических прав, Федеральным законом 1998 г. № 86-ФЗ «О лекарственных средствах», приказом Минздрава РФ 2003 г. № 266 «Об утверждении правил клинической практики в РФ». Все спортсмены были ознакомлены с правами пациента, предусмотренными законодательством, включались в исследование только после подписания информированного согласия. Проведенное исследование было одобрено локальным этическим комитетом.
Результаты исследования и их обсуждение
В течение исследования спортсменам было предложено трижды заполнить опросник: 1 -й опрос (визит 1) - перед началом курса лечения, 2-й опрос (визит 3) - после окончания лечения, 3-й (визит 4) - по истечении периода наблюдения (через 3 мес. после окончания лечения).
Значения показателей субшкал в отдельности и итоговый индекс шкалы КООS отражены в таблице 1.
Таблица 1.
Динамика показателей шкалы КООS
| Показатель | Основная группа (п=30) (Х±о) | Группа сравнения (п=30) (Х±о) | ||||
|---|---|---|---|---|---|---|
| Визит 1 | Визит 3 | Визит 4 | Визит 1 | Визит 2 | Визит 3 | |
| Боль | 75,6±12,9 | 79±11,2 | 84,3±10* | 75,0±20 | 79,5±14,2 | 75,8±12,7 |
| Симптомы | 54,4±8,1 | 61,9±10,7 | 69,7±10,1 | 54,9±13,9 | 60,1±13,8 | 57,7±7,9 |
| Ежедневная активность | 83,3±12,4 | 84,4±11,3 | 86,9±9,7 | 85,4±18 | 87,8±10,4 | 86,9±10,2 |
| Спортивная активность | 61,2±19,7 | 67,1±15,9 | 78,1±13,7 | 58,2±14,7 | 66,3±11,8 | 57,3±13,6 |
| Качество жизни | 62,9±18,1 | 69±14 | 78,9±11,3 | 61,9±18,2 | 67,7±13,1 | 64,7±12,9 |
| Итоговый индекс | 71,9±15,9 | 76±10,2 | 81,7±9 | 72,6±15,4 | 77±8,7 | 73,9±8,3 |
На рисунках 1-3 представлена графическая динамика показателей субшкал «Боль» и «Спортивная активность» как наиболее значимых в нашем исследовании, а также итогового индекса шкалы КООS.
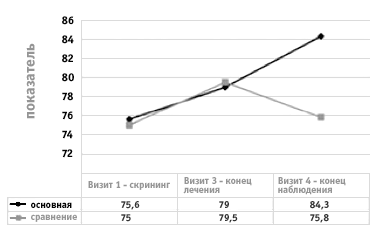
Рисунок 1.
Динамика показателей субшлалы «Боль»
в исследуемых группах
до и после лечения
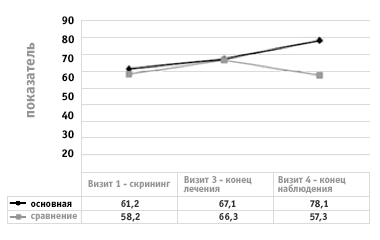
Рисунок 2.
Динамика показателей субшлалы «Спортивная активность»
в исследуемых группах
до и после лечения
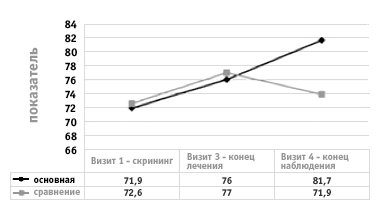
Рисунок 3.
Динамика суммарного индекса KOOS
в исследуемых группах
до и после лечения
Нами была проведена межгрупповая сравнительная оценка эффективности курса лечения препаратом Артрадол и курса физиотерапевтического лечения. Результаты статистической обработки отражены в таблице 2.
Таблица 2.
Значения показателей субшкал КOOS в исследуемых группах
| Название/ Итоговый индекс К00S | Основная группа (n=30) (Х±ơ) | Группа сравнения (n=30) (Х±ơ) | t-статистика (р=0,95, tгр. - 2,04) |
|---|---|---|---|
| Визит 1 | 71,9±15,9 | 72,6±5,9 | 2 |
| Визит 3 | 76±10,2 | 77±8,7 | 4 |
| Визит 4 | 81,7±9 | 73,9±8,3 | 22 |
Как видно из таблицы 2, различия значений итогового индекса КOOS между исследуемыми группами до начала терапии и после ее окончания статистически недостоверны
В результате тестирования силовых возможностей мышц разгибателей голени у спортсменов с посттравматической хондропатией коленного сустава с использованием изокинетической динамометрии нами получены следующие данные: средние значения ПВТ/ВТ (%) разгибателей поврежденная/интактная конечность на скорости 60° в основной группе составили
Таблица 3.
Силовая характеристика мышц разгибателей голени у спортсменов с посттравматической хондропатией коленных суставов до лечения
| Тестируемая угловая скорость | Основная группа (n=30) (Х±ơ) | Группа сравнения (n=30) (Х±ơ) | ||
|---|---|---|---|---|
| пораженная | интактная | пораженная | интактная | |
| 60° | 177±41,3 | 216,4±53,2 | 182,6±45,1 | 224,7±56,5 |
| 180° | 119,5±43,9 | 137,3±50,9 | 127,4±37,9 | 146,6±43,3 |
| 300° | 80,6±34,8 | 86,7±37,1 | 92,2±31,3 | 100,1±33,8 |
Сравнительный анализ силовых характеристик разгибателей голени показал асимметрию силы мышц разгибателей голени поврежденной и интактной конечностей на всех угловых скоростях: среднее значение дефицита силы разгибателей голени в обеих группах на скорости
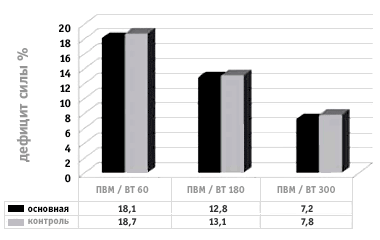
Рисунок 4.
Сравнительная оценка дефицита разгибателей
коленного сустава в исследуемых группах
до и после лечения
(травмированная / интактная нога)
При повторном изокинетическом тестировании после проведенного курса лечения нами получены следующие данные: средние значения ПВТ/ВТ (%) разгибателей поврежденная/интактная конечность на скорости 60° в основной группе составили
Таблица 5.
Силовая характеристика мышц разгибателей голени у спортсменов с посттравматической хондропатией коленных суставов после лечения
| Тестируемая угловая скорость | Основная группа (n=30) (Х±ơ) | Группа сравнения (n=30) (Х±ơ) | ||
|---|---|---|---|---|
| пораженная | интактная | пораженная | интактная | |
| 60° | 184,4±41,2 | 215±47,4 | 183,2±45,4 | 222,7±53,5 |
| 180° | 122,4±45,6 | 136,7±48,5 | 127,8±37,7 | 146,3±41,5 |
| 300° | 80,9±34,6 | 86,7±36,8 | 92,6±32,5 | 100,2±35,7 |
Графически изменение дефицита силовых характеристик мышц разгибателей голени в обеих группах после лечения представлено на рисунке 5.
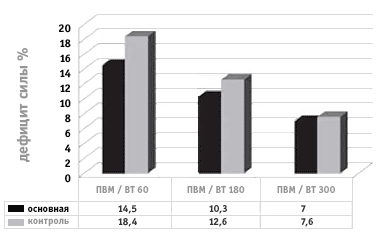
Рисунок 5.
Сравнительная оценка дефицита разгибателей
коленного сустава в исследуемых группах
до и после лечения
(травмированная / интактная нога)
Результаты статистической обработки и достоверность различий дефицита разгибателей мышц голени в исследуемых группах до и после лечения отражены в таблице 6.
Таблица 6.
Изменение дефицита силовых возможностей разгибателей коленного сустава в исследуемых группах до и после лечения
| Тестируемая угловая скорость | Основная группа (n=30) (Х±ơ) |
t-статистика (р=0,95, (tгр. - 2,04) |
Группа сравнения (n=30) (Х±ơ) |
t-статистика (р=0,95, (tгр. - 2,04) |
||
|---|---|---|---|---|---|---|
| до | после | до | после | |||
| 60° | 18,1±2 | 14,5±2,5 | 62 | 18,7±1,8 | 18,4±2,4 | 6 |
| 180° | 12,8±2,6 | 10,3±2,6 | 36 | 13,1±2,9 | 12,6±1,9 | 8 |
| 300° | 7,2±3,6 | 6,6±3,1 | 7 | 7,8±3,9 | 7,6±3,4 | 2 |
Таким образом, в результате повторного изокинетического тестирования нами выявлено положительное влияние лечения Артрадолом на функциональное состояние околосуставных мышц поврежденного коленного сустава, что проявляется в достоверном уменьшении дефицита силы разгибателей коленного сустава между поврежденной и интактной конечностью на угловых скоростях 60 и 180° (t>tгр =2,04). Изменение дефицита силы на угловой скорости 300° недостоверно (t< tгр =2,04).
Проведенное УЗИ гиалинового хряща коленных суставов у спортсменов с посттравматической хондропатией показало уменьшение его толщины в области нагружаемых поверхностей мыщелков бедренной кости, изменение его структуры в виде неровности, нечеткости контуров, повышения эхогенности, неоднородности эхоструктуры, индекс дегенеративного истончения хряща - от 0,55 до 0,75. Повторное УЗИ показало улучшение структуры суставного хряща в группе лечения Артрадолом: контуры суставного хряща стали более ровными и четкими, произошло увеличение ИДИХ; в группе сравнения изменений структуры хряща не выявлено. Динамика ИДИХ в исследуемых группах отражена в таблице 7.
Таблица 7.
Динамика индекса дегенеративного истончения хряща в исследуемых группах
| Параметры | ИДИХ (медиальный мыщелок) | ИДИХ (латеральный мыщелок) | ||
|---|---|---|---|---|
| до | после | до | после | |
| Основная группа | 59 | 64 | 61 | 66 |
| Группа сравнения | 72 | 72 | 73 | 73 |
Таким образом, нами выявлено ВыводыПолученные данные свидетельствуют о положительном влиянии курса лечения Артрадолом и курса магнитотерапии на функциональное состояние коленных суставов у спортсменов с посттравматической хондропатией по данным опросника KOOS. Однако по окончании периода наблюдения нами были отмечены дальнейшее улучшение функционального состояния коленных суставов в основной группе, что подтверждается улучшением показателей субшкал и итогового индекса КООS, и его снижение к исходному уровню в группе сравнения.
В результате проведенного двустороннего изокинетического тестирования мышц разгибателей коленного сустава нами выявлено улучшение биомеханических характеристик околосуставных мышц, что проявляется уменьшением асимметрии силы четырехглавой мышцы между поврежденной и интактной конечностью.
По нашему мнению, это влияние является косвенным и связано с симптом-модифицирующим действием препарата Артрадол, проявляющимся в уменьшении болевого синдрома, что, в свою очередь, позволяет спортсмену развивать максимальную силу. УЗИ гиалинового хряща коленных суставов у спортсменов с посттравматической хондропатией показало, что под влиянием лечения Артрадолом произошли улучшение его структуры, а также увеличение индекса дегенеративного истончения. В группе сравнения изменений структуры и толщины суставного хряща не выявлено.
Таким образом, мы считаем, что применение Артрадола в комплексном восстановительном лечении спортсменов с посттравматической хондропатией - эффективный и безопасный метод. Лечение Артрадолом не ограничивает возможность спортсменов тренироваться и участвовать в соревнованиях, что является немаловажным фактором их профессиональной деятельности. Также хондропротективная терапия служит профилактической мерой, снижающей риск развития посттравматического остеоартроза.
- Арьков В.В. Показатели изокинетческой динамометрии мышц бедра у спортсменов после реконструкции передней крестообразной связки коленного сустава
/В.В. Арьков, О.Н. Миле¬нин, З.Г. Орджоникидзе
//Лечебная физкультура и спортивная медицина. 2011. № 12(96). С. 23-26.2. - Бакарджиева АН., Дьячков КА МРГ и УЗИ-параллели в оценке внутрисуставных структур у больных с закрытыми повреждениями коленного сустава до и после артроскопии
//Г?ний ортопедии. 2010. № 2. С. 96-102.3. - Гзрасименко МА Диагностика и лечение повреждений и ортопедических заболеваний ко¬ленного сустава
/ МА Герасименко, кВ. Белецкий. Минск: Тэхналопя, 2010. 167 с.4. - Ермак ЕМ. Современные ультразвуковые технологии в диагностике деструктивных и репа- ративных процессов в костной и хрящевой тканях: Дисс. ...д-рамед. наук. Челябинск, 2005. 235 с.5.
- Еськин НА, Атабекова Л А, Бурков С.Г. Ультрасонография коленных суставов (методика и ультразвуковая анатомия) // SonoAce International. 2002. № 10. С. 85-92.6.
- Миронов С.П., Еськин НА, Орлецкий АК, Цыкунов М.Б. Новый метод тестирования с по¬мощью сонографии при повреждении связок коленного сустава // Тез. докл. VI конгресса Ев¬ропейского общества спортивной травматологии и артроскопии каленного сустава. Берлин, 1994. С. 43.7.
- Насонова В А Остеоартроз каленного сустава: причины развития, диагностика и профилак¬тика/В А. Насонова//Consilium medicum. 2003. № 5. С. 87-92.8.
- Новик АА, Ионова Т.И. Руководство по исследованию качества жизни в медицине/под ред. академика РАМН ЮЛ. Шевченко. М: ОЛМА-Медиагрупп, 2007. С. 169-170.9.
- СенчаАН., Беляев Д.В., Чижов ПА Ультразвуковая диагностика. Коленный сустав/АН. Сенча, Д.В. Беляев, ПА Чижов. М.: Издательский дом «Видар-М», 2012.200 с.10.
- Ультразвуковое исследование и магнитно-резонансная томография в оценке характера из¬менений суставов при псориатическом артрите / НЛ Климентенко, ВД. Завадовская, П.Н. Пестерев, Т.Б. Перова, Н.Г. Завьялова, Т.В. Жогина, О.Ю. Бородин//Медицинская визуали¬зация. 2011. №5. С. 84-92.11.
- Цыкунов М.Б. Ультразвуковая диагностика повреждений коленного сустава у спортсменов /М.Б. Цыкунов, НА Болин, АК. Орлецкий//Вести, спорте, медицины России. 1993. №2-3. С. 81.12.
- Buckwalter JA Articular cartilage: degeneration and osteoarthritis, repair, regeneration, and transplantation/J.A Buckwalter, H.J. Mankin//Instr. Course. Led. 1998. Vol. 4. № 7. P. 487-504.13.
- Brandt K.D. Is a strong quadriceps muscle bad for a patient with knee osteoarthritis? Text./KD. Brandt //Ann. Intern. Med. 2003. Vol. 138. P. 678-679.14.
- Campo G.M., Avenoso A, Campo S. et at. Chondroitin sulfals: antioxidant properties and bene¬ficial effects // Mini Rev Med Chem. 2006. Vot.6(12). P. 1311-1320.15.
- Hunziker EB. Articular cartilage repair: basic science and Meal progress. A review of the cur¬rent status and prospects //EB. Hunziker//Osteoarthritis Cartilage. 2002. № 10. P. 1432-1463.16.
- Hurley M.V. Improvements in quadriceps sensorimotor function and disability of patients with knee osteoarthritis Mowing a clinically practicable exercise regime /M.V. Hurley, D.L Scott//Br. J. of Rheum. 1998. -ol. 37. P. 1181-1187.17.
- Knee injury and osteoarthritis outcome score (KOOS) development of a self-administered outco¬me measure/ EM. Roosetai.//J. Orthop. Sports Phys. Ther. 1998. Vol. 28. P. 88-96.18.
- Lewek M.D. Quadriceps femoris muscle weakness and activation failure in patients with sympto¬matic knee osteoarthritis Text./M.D. Lewek, KS. Rudolph, L Snyder-Madder//J. Orthop. Res. 2004. Vol. 22. P. 110-115.19.
- Martel-Pelletier J., Lajeunesse D., Pelletier J.P. Etiopathogenesis of osteoarthritis.ln: Arthritis md Ailed Conditions: A Textbook of Rheumatology. W.J. Koopman, L.W. Moreland (edsj. Baltimo¬re: lippincott, Wikmgs №, 2005. P. 2199-2296.20.
- NietsenA.B., YdeJ. Epidemiology and traumatolog soccer II Am//J. Sports Med. 1989. Vol. 17. P. 803-807.21.
- Outcome of untreated traumatic articular caiWage defects of the knee: a natural history study/ K.D. Shelboume et al. //J Bone Joint Surg Am. 2003. №85. P. 8-16.22.
- Reachenbach S., Sterchl ft, Scherer M. et al. Meta-analysis: Chondroitin lor osteoarthritis oft- he knee and hip //Ann. Int. Med. 2007. Vol. 146. P. 580-590.23.
- Stemenda C., Heilman D., Brandt K.D. etal. Reduced quadriceps strength relative to body we- igth: a risk factor for knee osteoarthritis in women?//Arthritis Rheum. 1998.Ш41.Р. 1951-1959.24.
- The Epidemiology, Biology, Diagnosis and Treatment of Osteoarthritis of the Knee/W.P. Micha¬el et al.//Dtsch. Arztebl. Int. 2010. № 107. P. 152-162.25.
- Zhang W., Doherty М., Leeb B.F. et al. EULAR evidence based recommendations for the mana- gementof hand osteoarthritis: report of task force of the EULAR Standing Committee for Intematio- nalClinical Studies Including Therapeutic (ESCISIT)//Ann. Rheum. Us. 2007. Vol. 66. P. 377-388.